醫療保健合規袖珍指南
已發表: 2020-06-26醫療保健是受到數字技術轟炸的主要行業之一,旨在實現其基礎設施景觀和服務的現代化。
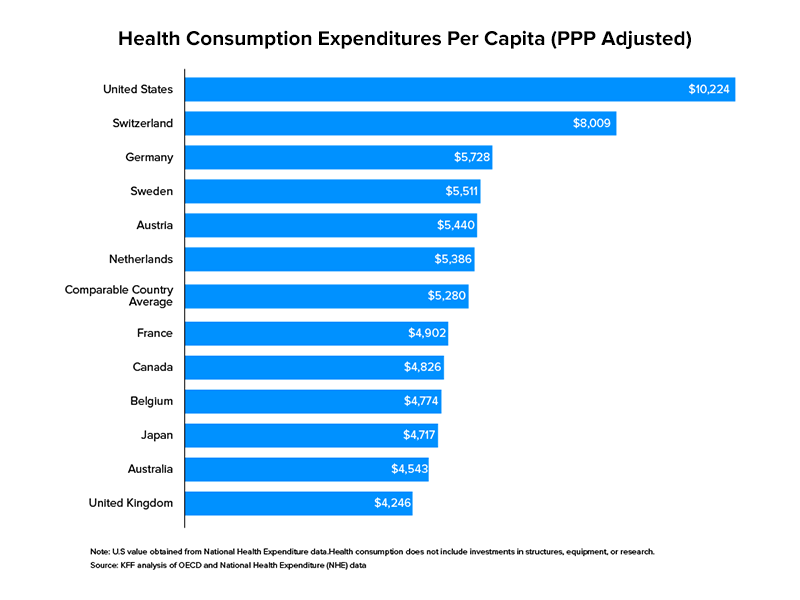
以機構支出為衡量標準,與其他行業相比,醫療保健在美國政府支出中遙遙領先。 2017年,美國為醫療保健撥款3.5萬億美元。 作為該國國內生產總值的一部分,這達到了17.7% 。 在美國,醫療保健不僅僅局限於擁有大量資本進行投資和擴張的傳統企業,而是向所有人開放以供參與。
數字健康是該行業的一個發展前景,包括遠程醫療、通過智能手機應用程序進行遠程監控和處方藥上門交付等商業模式。 僅在 2019 年,倡導數字醫療保健採用的初創公司在美國境內的 1,700 多項交易中籌集了超過170 億美元。 正如預期的那樣,移動醫療保健的發展正在成為中心舞台。
開發聲稱可以影響/改善個人衛生的產品是一個難以破解的難題,這不是因為所涉及的醫療保健軟件開發服務挑戰,而是因為信託指南。
多虧了我們的合作夥伴,Appinventiv 處於這一變革的前沿,推動了行業的心跳。 作為一家醫療保健應用程序開發公司,我們一直在那裡並做到了這一點,這對於將突破性的想法付諸實踐是必要的。 作為您的知己,今天我們將討論您在開發 mHealth 應用程序時必須牢記的常見法規和合規性。
什麼是醫療保健法規合規性?
醫療保健中的法規遵從性是指醫療協會遵守適用於其業務流程的法律、指南、法規和規範。 違反監管合規通常會導致法律處罰,包括聯邦罰款。 它是滿足或超過與特定醫療保健協會或供應商相關的合法、道德和專業規範的連續循環。
目前,醫院和醫療保健提供者等醫療保健公司都有專門的團隊成員,他們特別關注法規遵從性。 醫院監管要求的原因和本質優勢是改善患者護理。
醫療保健合規的目的是什麼?
醫療保健合規性是每個醫療提供者的基本部分。 這是遵循與醫療保健服務實踐相關的規則、指南、法律和法規的方式。
醫療保健的合規性涵蓋了廣泛的實踐,並遵守內部和外部規則。 然而,大多數醫療服務合規性問題與患者安全、患者數據保護和計費演練有關。
美國衛生與公眾服務部 (HHS) 制定了全國范圍的標準,稱為《健康保險流通與責任法案》(HIPAA),醫療合規的核心特徵是支持該立法。
為什麼醫療保健合規很重要?
合規性使任務順利進行,並確保每個人都遵循合法程序並理解假設。
然而,與不同行業相比,醫療服務的合規性所帶來的風險要高得多。 另一方面,如果像醫生和護士這樣的醫療從業者不遵循合法程序,那麼他們最終可能會傷害患者或其他工作人員。
歸根結底,醫療保健合規性是關於提供安全、高質量的患者護理。 遵守行業標準和法規有助於醫療保健組織繼續提高護理質量。
最後,醫療保健合規性是關於提供受保護的、優質的、安全的患者護理。 遵守行業指南和法規有助於醫療保健組織不斷提高護理質量。
醫療機構必須遵守政府的嚴格指導方針、法律和法規。 違反這些法律可能會招致訴訟、巨額罰款,甚至吊銷執照。
合規問題的高風險是什麼?
監管框架作為用於製裁指導方針的模型。 這樣的結構可能會在明確的興趣領域內創建,例如醫療保健行業。 政府經常依賴利用這些框架來製定和頒布指導方針、規則和法律。 監管框架通常首先在考慮最終目標的情況下制定。
讓我們來看看困擾每個人的主要問題,那就是醫療保健中的合規性問題是什麼?
HIPAA 和數據洩露
基於價值的補償安排
反回扣和醫生醫院問題
盡職調查流程
遠程醫療提供者資格
恢復審計承包商
免稅醫院和合規要求
美國的醫療保健法規和合規性
數字健康對健康信息技術 (HIT)、移動健康、個性化處方、可穿戴技術和遠程健康有詳細的說明。 移動應用程序是最常見的醫療保健交付方式之一,無論是通過離線在線服務還是軟件即服務。 如果是這種情況,企業家必須提出以下問題並找到客觀答案:

上述調查問卷將確定您的移動應用程序是否需要信託許可。 如果您的回答大多是肯定的,那麼有三個聯邦機構會調查您的移動醫療產品問題:
- 食品和藥物管理局 (FDA)
- 聯邦貿易委員會 (FTC)
- 民權辦公室 (OCR)
下面我們來看看關鍵的聯邦職能領域以及醫療軟件開發公司必須為其客戶提供建議的細粒度事實檢查的範圍。
1. 健康保險流通與責任法案 (HIPAA)
該法案由美國衛生與公眾服務部的民權辦公室 (OCR) 執行。 此符合醫療標準的HIPAA 安全規則保護符合條件的健康相關數據的隱私和安全問題,在特定情況下,認為報告數據洩露是強制性的。 不遵守特定的 HIPAA 安全規則可能會導致罰款,最低支付100美元,每次違規的罰款高達150 萬美元。
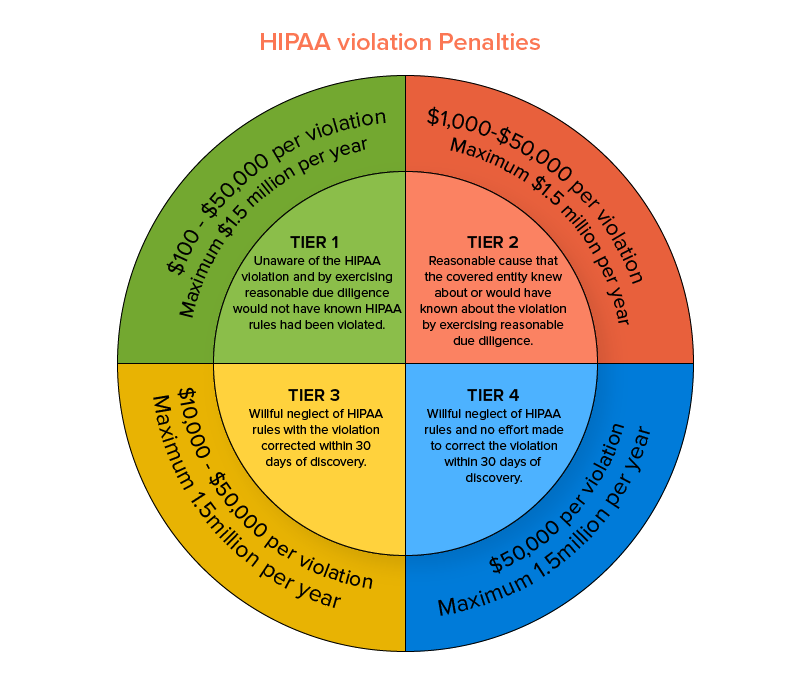
既然您已經清楚地了解了滿足醫療保健法規要求的嚴肅性,我們應該繼續研究應該符合 HIPAA 傳統政策的醫療應用程序類型。 三個 3 因素決定了應用程序在操作方面被區分為醫療的資格標準:
I. 使用應用程序的實體的性質。
實體是指將使用該應用程序的客戶。 HIPAA 的憲法涵蓋了一組預定義的醫療從業人員,例如醫生、醫生、醫院等組織和健康保險提供者。 如果他們是該應用程序的直接受益者,則必須逐字遵循 HIPAA的醫療保健法規和醫院法規遵從列表。 另一方面,如果該應用程序只是策劃並與客戶分享衛生提示或健康知識,則將不受 HIPAA 章程的約束。
二、 應用程序產生、保存和進一步共享的數據的性質。
數據對於在線業務的運作需求至關重要。 聯邦當局推動制定法律,以消除數據洩露等安全問題,並確保存在強大的加密基礎設施。 從本質上講,收集的數據不應該也不應該通過他們的個人信息(如地址、社會安全號碼等)將惡意行為者引向人們。如果應用程序要處理這些個人信息的使用,則 HIPAA 規則將應用。

三、 為應用程序提供動力的底層軟件。
最佳醫療保健移動應用程序開發必須專注於創新安全手機應用程序。 HIPAA 共享受保護的健康信息 (PHI) 的詳細信息,並指導軟件供應商圍繞它建立安全網。 其指令有一份詳盡的審計清單和要為 PHI 安裝的內部控制。
2. 聯邦貿易委員會法(FTC 法)
該法案規定了監管協議,以處理企業中的不公平索賠和不當行為,還涉及隱私問題和一般數據安全挑戰。 該法律涵蓋有關應用程序使用的毫無根據的聲明。 FTC 的健康違規通知規則要求選定的企業報告個人健康記錄等數據洩露。
3. 聯邦食品、藥品和化妝品法案 (FD&C Act)
本法委託食品藥品監督管理局實施。 他們的主要目標是確保醫療設備(包括移動應用程序)符合標準指南,因此可以安全地大量使用。 最重要的是,我們提到並非所有醫療保健應用程序都屬於這個管轄範圍,而是少數幾個。 這些是如果未能兌現索賠會對消費者健康造成嚴重後果的那些。
附加規定 對於數字健康
雖然上述行為是針對醫療保健應用的,但還有其他一些行為並非出於此原因而進行了調整,以包含相同的內容。 在本節中,我們將概述移動醫療企業家必須遵守的此類國家支持的規範。
1. 食品藥品監督管理局 (FDA)
美國食品和藥物管理局是美國政府支持的機構,是美國衛生與公眾服務部的重要組成部分。 醫療保健應用程序開發人員在設計應用程序以獲得 FDA 許可時必須注意這樣一套定義明確的指南。 對於數字健康領域,FDA 根據以下兩個假設將移動應用程序歸類為“醫療”板塊:

- 該應用程序可作為附件與已受監管的醫療設備一起使用。
- 該應用程序將移動平台轉變為受監管的移動設備
基於上述一級分類,應用程序的子行業是根據其與以下新興數字技術的關係來定義的,以接近 FDA 的批准。
I. 軟件作為醫療設備 (SaMD)
SaMD 被定義為一種模型,其中軟件用於醫療目的而不與硬件醫療儀器/設備相關聯。 該模型高度靈活,可應用於從虛擬網絡到醫療設備的一系列平台。
國際醫療器械監管機構論壇 (IMDRF) 是一個倡導對醫療器械進行系統治理的全球聯盟。 2013 年,它制定了作為醫療器械工作組 (SaMDWG) 的軟件,以引入可操作的指導,以支持該領域數字技術的進步。 該小組由 FDA 本身領導,記錄了大量關於以下方面的框架:
- 定義
- 風險分類
- 質量管理體系
- 臨床評估
瀏覽他們的目錄將幫助您確定是否會獲得 SaMD 批准。
二、 無線醫療設備
是指具備無線傳輸信息斜線數據以促進醫療保健服務的醫療設備。 此類工具包部署無線電頻率進行通信,可通過 WiFi、藍牙或智能手機進行傳輸。 一個常見的例子是射頻識別 (RFID) 設備,您可能會在公司辦公室找到。

三、 遠程醫療
健康 IT 分為遠程醫療和遠程醫療,以簡化獲得 FDA 批准的過程。 遠程醫療被指定為使用電信來促進和支持與醫療保健相關的功能——自 COVID-19 爆發以來,這一功能越來越受到關注。 一家定制的醫療保健軟件開發公司可以開發應用程序,這些應用程序使用:
- 實時(異步)視頻會議
- 存儲轉發(異步)視頻會議
- 遠程病人監護 (RPM)
- 移動健康 (mHealth)
四。 健康資訊科技
在這種情況下,我們最好引用聯邦政府健康信息技術國家協調員辦公室提供的定義,“硬件、軟件、集成技術或相關許可、知識產權、升級或作為服務出售的打包解決方案旨在或支持醫療保健實體或患者使用電子方式創建、維護、訪問或交換健康信息。”
五、醫療器械數據系統(MDDS)
可用於傳輸數據、保存/存儲信息、將數據從一種格式轉換為另一種格式或僅顯示科學/醫學數據的硬件/軟件產品屬於 MDDS 類別。 此類設備的目的不是提供額外的特徵或增強數據集,而是簡單地顯示它。
六、 醫療設備互操作性 (MDI)
可以說,沒有其他數字健康子域比 MDI 更能說明安全電話應用程序的概念。 醫療設備互操作性是指多個設備之間的跨平台/技術信息交換。 與主要動機是演示的 MDDS 不同,MDI 應用程序可以顯示、存儲和分析數據。 由於來回通信,它們還可以用於控制其他產品。
七。 設備軟件功能
在談論這一類別時,僅對那些根據 FDA 指南有資格成為“設備”的軟件應用程序給予許可。 具有最小或沒有消費風險的軟件設備可能不需要 FDA 的官方批准,並且該組織在這種情況下明確表示它
“將行使執法自由裁量權,不會期望製造商提交上市前審查申請或向 FDA 註冊和列出他們的軟件。 ”
八。 網絡安全
網絡安全本身並不是 mHealth 應用程序的一種分類模式。 然而,FDA 希望建立一個明確的諒解備忘錄 (MOU),以便它可以權衡應用程序帶來的數據安全挑戰和對用戶的好處。
九。 人工智能/機器學習
與其他技術相比,人工智能對醫療保健的影響不成比例地巨大。 然而,由於 FDA 不得不對其監管框架進行調整,這一領域的進展是相當近期的。 根據其最新指南,FDA 將與製造商攜手合作,從其上市前開發階段開始持續評估軟件,並在上市後性能階段達到高潮。 該框架特別適用於 SaMD。
2. HL7 標準
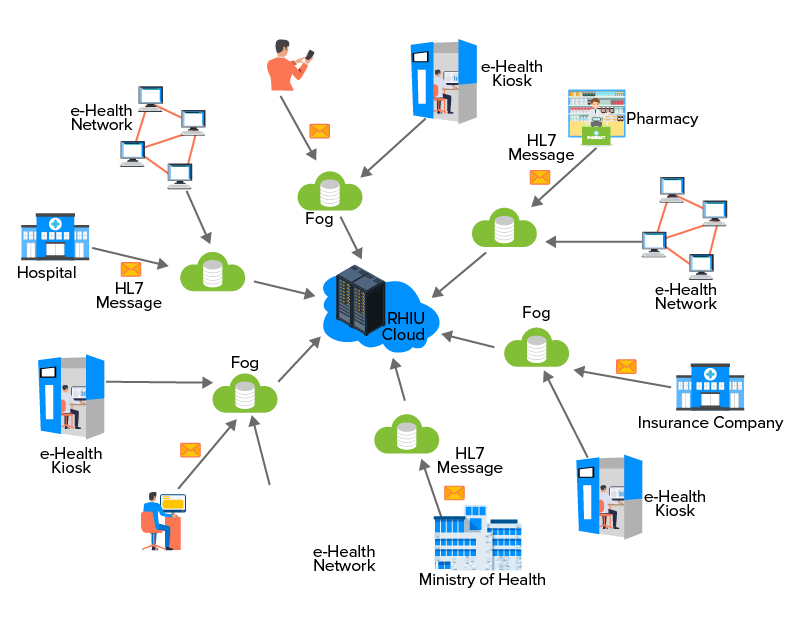
Health Level Seven International,簡稱 HL7,是一個成立於 1983 年的非營利組織,它為電子健康信息的交換、集成、共享和檢索制定行業基準,以實現程序性醫療實踐。 除此之外, HL7 標准在管理健康服務、保持無縫醫療保健交付和評估結果方面發揮著基本作用。
他們是怎麼做到的?
HL7 標准定義了兩個醫療保健應用程序之間可互操作的信息打包,規定了語言、數據格式及其結構的工作流程,以便輕鬆集成到系統中。 通過這樣做,他們減少了對技術基礎設施的投資,並使患者受益,從而使醫療保健更加負擔得起。 遵守起草的規則以獲得 HL7 批准對於規範醫療保健行業具有雙重好處。 首先,醫療保健應用程序已被普遍接受並準備在全球範圍內部署。 其次,降低了應用開發成本。
3. HITECH法案
2009 年巴拉克奧巴馬總統執政期間引入了經濟和臨床健康信息技術法案。HITECH 法案的目的是通過電子健康記錄 (EHR) 促進企業採用健康信息技術。 政府還收緊了圍繞 1996 年 HIPAA 法案的鬆散端,此後,醫療保健企業必須在其憑證被盜用時通知客戶。
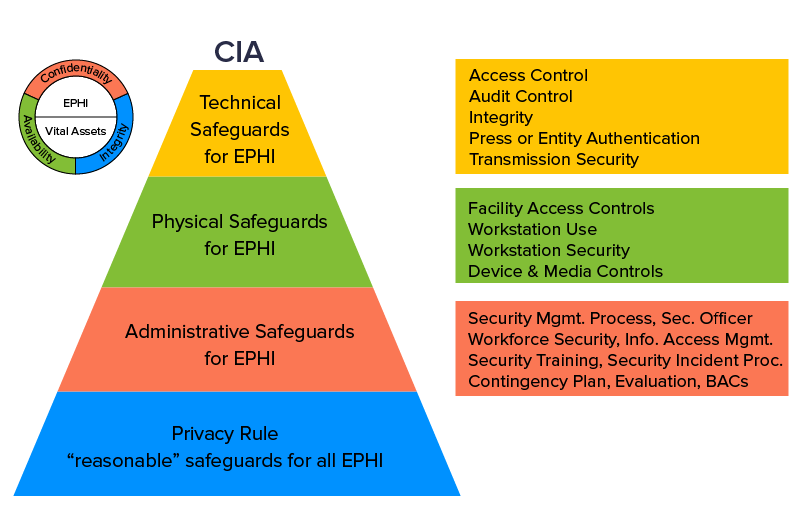
HITECH 法案的直接影響是,借助 EHR,兩個不同實體之間的信息共享變得更容易處理。 該法案還確保安裝難以破解的安全基礎設施與 HIPAA 法案的隱私和安全必備條件相一致。 獲得 HITECH 批准的所有監管要求都通過最終綜合規則納入 HIPAA,這導致兩種行為都在單一立法下疊加。
4. 自帶設備
自帶設備 (BYOD) 是一種概念性實踐,醫療保健雇主允許醫務人員使用個人設備,例如但不限於智能手機和平板電腦來執行公務。 如果您的 mHealth 解決方案未針對 BYOD 安全協議進行定制,事情可能會瞬間走下坡路。 例如,假設員工丟失了他/她的智能手機,而該設備可以訪問關鍵的受保護健康信息 (PHI)。
這就是經過深思熟慮的移動設備管理策略發揮作用的地方。 如果應用程序開發人員在 mHealth 解決方案中內置了遠程擦除功能,您就可以擦除與丟失設備相關的數據。 BYOD 保護傘中的類似功能包括保護電子郵件和瀏覽器等客戶端應用程序。 在初始 SDLC 階段注意這些細節可以幫助初創公司最終獲得 BYOD 批准。
5. GDPR
通用數據保護條例由歐盟 (EU) 制定,適用於收集和處理歐盟公民客戶數據的智能手機應用程序。 談到在歐盟以外的工作中該法案的類似迭代,它被認為是應用程序開發人員根據相同創建移動醫療解決方案的一種安全措施。 隱私保護是 GDPR 的本質,聯邦當局通過它試圖(成功地)將一些個人數據的控制權交給外行。 它還公開了與私有數據管理有關的業務實踐。

GDPR 的規定要求移動應用程序在收集或處理其數據之前請求許可,即主動用戶同意。 該應用程序應該使用戶可以通過複選框或任何其他按鈕輕鬆分享他們的協議,以單擊並註冊操作。 此外,不應預先勾選此類複選框,以免在心理上影響用戶的選擇,而用戶的選擇必須不受阻礙。 條款和條件頁面必須有自己的“我同意”按鈕。 GDPR 在很大程度上使個人數據控制民主化,因為即使在用戶同意後,如果用戶選擇,他們也可以撤銷授予應用程序的所有權利並退出。 如果移動應用程序開發公司根據此討論設計解決方案,則從當局激活 GDPR 批准相對容易。
最後的想法
得益於移動醫療、遠程醫療、傳感器和可穿戴技術以及遠程監控工具等數字技術,到 2026 年,全國醫療保健支出預計將達到 5.7 萬億美元。 這種醫療保健趨勢表明,前所未見的醫療解決方案正在艱難前進,這些解決方案結合了技術,可以立即向公眾推廣。 他們還有望使所有人都能負擔得起醫療保健作為一項基本權利,而不是一項可以使用的服務。 當您專注於企業的業務方面時,讓美國頂級醫療保健應用程序開發機構之一的Appinventiv作為您的技術指南隨時待命。
我們將等待聽到您的想法。
